Page 20 - RCOE 22-1
P. 20
INVESTIGACIÓN BÁSICA
➤➤ 20
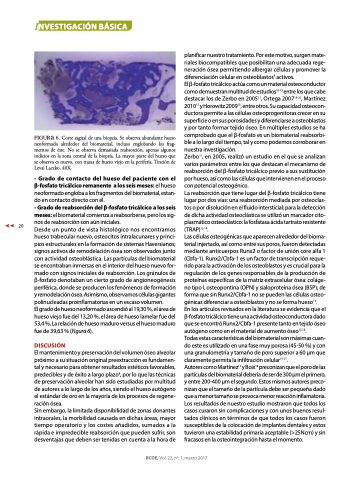
FIGURA 6. Corte sagital de una biopsia. Se observa abundante hueso neoformado alrededor del biomaterial, incluso englobando los frag- mentos de éste. No se observa demasiada reabsorción, apenas algunos indicios en la zona central de la biopsia. La mayor parte del hueso que se observa es nuevo, con trazas de hueso viejo en la periferia. Tinción de Levai Laczko, 40X.
- Grado de contacto del hueso del paciente con el β-fosfato tricálcico remanente a los seis meses: el hueso neoformado engloba a los fragmentos del biomaterial, estan- do en contacto directo con él.
- Grado de reabsorción del β-fosfato tricálcico a los seis meses: el biomaterial comienza a reabsorberse, pero los sig- nos de reabsorción son aún iniciales.
Desde un punto de vista histológico nos encontramos hueso trabecular nuevo, osteocitos intralacunares y princi- pios estructurales en la formación de sistemas Haversianos; signos activos de remodelación ósea son observados junto con actividad osteoblástica. Las partículas del biomaterial se encontraban inmersas en el interior del hueso nuevo for- mado con signos iniciales de reabsorción. Los gránulos de β-fosfato denotaban un cierto grado de angioneogénesis periférica, donde se producen los fenómenos de formación y remodelación ósea. Asimismo, observamos células gigantes polinucleadas proinflamatorias en un escaso volumen.
El grado de hueso neoformado ascendió al 19,30 %, el área de hueso viejo fue del 13,20 %, el área de hueso lamelar fue del 53,4 %, La relación de hueso maduro versus el hueso maduro fue de 39,63 % (Figura 6).
DISCUSIÓN
El mantenimiento y preservación del volumen óseo alveolar próximo a su situación original preextracción es fundamen- tal y necesario para obtener resultados estéticos favorables, predecibles y de éxito a largo plazo8, por lo que las técnicas de preservación alveolar han sido estudiadas por multitud de autores a lo largo de los años, siendo el hueso autógeno el estándar de oro en la mayoría de los procesos de regene- ración ósea.
Sin embargo, la limitada disponibilidad de zonas donantes intraorales, la morbilidad causada en dichas áreas, mayor tiempo operatorio y los costes añadidos, sumados a la rápida e impredecible reabsorción que pueden sufrir, son desventajas que deben ser tenidas en cuenta a la hora de
planificar nuestro tratamiento. Por este motivo, surgen mate- riales biocompatibles que posibilitan una adecuada rege- neración ósea permitiendo albergar células y promover la diferenciación celular en osteoblastos9 activos.
El β-fosfato tricálcico actúa como un material osteoconductor como demuestran multitud de estudios10-15 entre los que cabe destacar los de Zerbo en 200511, Ortega 200719-20, Martínez 201012 yHorowitz200913,entreotros.Sucapacidadosteocon- ductora permite a las células osteoprogenitoras crecer en su superficie o en sus porosidades y diferenciarse a osteoblastos y por tanto formar tejido óseo. En múltiples estudios se ha comprobado que el β-fosfato es un biomaterial reabsorbi- ble a lo largo del tiempo, tal y como podemos corroborar en nuestra investigación.
Zerbo11, en 2005, realizó un estudio en el que se analizan varios parámetros entre los que destacan el mecanismo de reabsorción del β-fosfato tricálcico previo a sus sustitución por hueso, así como las células que intervienen en el proceso con potencial osteogénico.
La reabsorción que tiene lugar del β-fosfato tricálcico tiene lugar por dos vías: una reabsorción mediada por osteoclas- tos o por disolución en el fluido intersticial; para la detección de dicha actividad osteoclástica se utilizó un marcador cito- plasmático osteoclástico: la fosfatasa ácida tartrato resistente (TRAP)12-14.
Las células osteogénicas que aparecen alrededor del bioma- terial injertado, así como entre sus poros, fueron detectadas mediante anticuerpos Runx2 o factor de unión core alfa 1 (Cbfa-1). Runx2/Cbfa-1 es un factor de transcripción reque- rido para la activación de los osteoblastos y es crucial para la regulación de los genes responsables de la producción de proteínas específicas de la matriz extracelular ósea: coláge- no tipo I, osteopontina (OPN) y sialoproteína ósea (BSP); de forma que sin Runx2/Cbfa-1 no se pueden las células osteo- génicas diferenciar a osteoblastos y no se forma hueso13.
En los artículos revisados en la literatura se evidencia que el β-fosfato tricálcico tiene una actividad osteoconductora dado que se encontró Runx2/Cbfa-1 presente tanto en tejido óseo autógeno como en el material de aumento óseo15,16.
Todas estas características del biomaterial son máximas cuan- do este es utilizado en una fase muy porosa (45-50 %) y con una granulometría y tamaño de poro superior a 60 μm que claramente permita la infiltración celular15-21.
Autores como Martínez12 y Boix18 preconizan que el poro de las partículas del biomaterial debería de ser de 300 μm el primero, y entre 200-400 μm el segundo. Estos mismos autores preco- nizan que el tamaño de la partícula debe ser pequeña dado que a menor tamaño se provoca menor reacción inflamatoria. Los resultados de nuestro estudio mostraron que todos los casos curaron sin complicaciones y con unos buenos resul- tados clínicos en términos de que todos los casos fueron susceptibles de la colocación de implantes dentales y estos tuvieron una estabilidad primaria aceptable (>25Ncm) y sin fracasos en la osteointegración hasta el momento.
RCOE, Vol. 22, no. 1, marzo 2017