Page 25 - RCOE 25-2
P. 25
en distintos tratamientos de Odontología4.
En la actualidad la utilización de Fibrina rica en pla- quetas y leucocitos, en lugar de plasma rico en pla- quetas, tiene su base en la capacidad de la primera de generar un coágulo mucho más estable y firme, lo cual facilita su manipulación en el área del defecto tisular, manteniendo los factores biológicos al igual que el PRP, pero en mayor proporción, obtenida por un pro- tocolo más estricto, mayor rapidez de manipulación y obtención, permanencia prolongada in vivo, al tiempo que facilita una clara reducción de costes5,6.
Esta técnica (L-PRF) tiene una clara indicación en implantología y cirugía bucal, especialmente en téc- nicas complementarias de regeneración. Ha sido utili- zada con excelentes resultados clínicos en las técnicas de elevación de seno maxilar, en las que se ha podido comprobar que puede estimular de manera signi- ficativa la formación de hueso y la angiogénesis de los tejidos en las perforaciones de la membrana de Schneider8,9.
Igualmente para su utilización en las técnicas de regeneración ósea en cirugía bucal, resulta esencial la acción de la conocida proteína RUNX2, considera- da un factor de transcripción clave vinculado con el proceso de diferenciación de los osteoblastos. Hoy sabemos que, la progresiva liberación de estas proteí- nas, que se encuentran en la matriz de la fibrina, tiene entre otras funciones, la de promover la migración celular de estructuras como el ligamento periodontal y los fibroblastos gingivales10.
También se ha descrito la utilización de esta técnica en alvéolos post extracción, evaluándose la formación de hueso seis semanas tras su utilización y sin signos de reabsorción ósea. Tal como ocurre en el caso clínico que presentamos, cuando una o más paredes están ausentes o parcialmente reabsorbidas, es recomen- dable la utilización combinada de L-PRF y sustitutos óseos, demostrando su gran capacidad de actuar como conector biológico entre las partículas óseas.
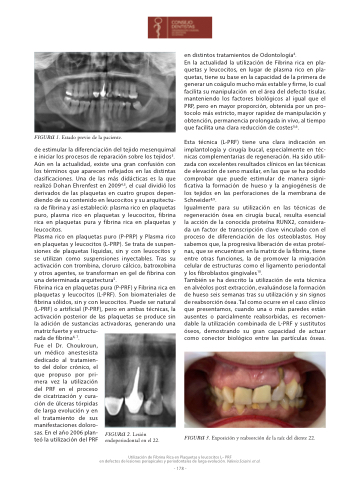
FIGURA 3. Exposición y reabsorción de la raíz del diente 22. Utilización de Fibrina Rica en Plaquetas y leucocitos L– PRF
en defectos de lesiones periapicales y periodontales de larga evolución. Valeria Sciaini. et al. - 178 -
FIGURA 1. Estado previo de la paciente.
de estimular la diferenciación del tejido mesenquimal e iniciar los procesos de reparación sobre los tejidos5. Aún en la actualidad, existe una gran confusión con los términos que aparecen reflejados en las distintas clasificaciones. Una de las más didácticas es la que realizó Dohan Ehrenfest en 20094,5, el cual dividió los derivados de las plaquetas en cuatro grupos depen- diendo de su contenido en leucocitos y su arquitectu- ra de fibrina y así estableció: plasma rico en plaquetas puro, plasma rico en plaquetas y leucocitos, fibrina rica en plaquetas pura y fibrina rica en plaquetas y leucocitos.
Plasma rico en plaquetas puro (P-PRP) y Plasma rico en plaquetas y leucocitos (L-PRP). Se trata de suspen- siones de plaquetas líquidas, sin y con leucocitos y se utilizan como suspensiones inyectables. Tras su activación con trombina, cloruro cálcico, batroxobina y otros agentes, se transforman en gel de fibrina con una determinada arquitectura5.
Fibrina rica en plaquetas pura (P-PRF) y Fibrina rica en plaquetas y leucocitos (L-PRF). Son biomateriales de fibrina sólidos, sin y con leucocitos. Puede ser natural (L-PRF) o artificial (P-PRF), pero en ambas técnicas, la activación posterior de las plaquetas se produce sin la adición de sustancias activadoras, generando una matriz fuerte y estructu-
rada de fibrina6, 7.
Fue el Dr. Choukroun, un médico anestesista dedicado al tratamien- to del dolor crónico, el que propuso por pri- mera vez la utilización del PRF en el proceso de cicatrización y cura- ción de úlceras tórpidas de larga evolución y en el tratamiento de sus manifestaciones doloro- sas. En el año 2006 plan- teó la utilización del PRF
FIGURA 2. Lesión endoperiodontal en el 22.